近日,国家自然科学基金委发布项目获批通知。西安交通大学第一附属医院心内科2024年再创佳绩,荣获包括1项重点项目、1项杰出青年基金和1项国际合作项目在内的11项基金。其中,心血管病医院院长袁祖贻教授作为负责人申请的重点项目、吴岳教授作为负责人申请的杰出青年基金项目、以及王胜鹏教授作为负责人申请的重大国际(地区)合作项目均获批;同时郭宁教授等获批面上及青年项目等共8项,系医院心内科近年获批国科金的最佳成绩。
在基础研究方面,袁祖贻、吴岳教授团队在微生物代谢和心血管药物互作机制方面取得系列重要进展,2024年上半年在Cell子刊Cell Metabolism(影响因子:29.0)、Cell Host Microbe(影响因子30.3),及Journal of Hepatology (影响因子:25.7),以及Cir Res和JCI等发表系列论著,受到国际学术界关注。
心血管疾病多为慢性病,需要长期口服药物进行一级和二级预防,每年心血管疾病口服药物消耗达上千亿,但其疗效和副作用因人而异。近期研究逐渐发现,这种药效变化可能同肠道菌群的功能差异有关。口服药物科引起菌群的代谢功能改变:药物进入肠道,造成菌群的谱型、分布、功能变化,从而导致菌群的次生代谢产物变化,如胆汁酸、短链脂肪酸、氨基酸等等,后者可能调控疾病的进程,也影响药物的药效和副作用。
他汀类药物是治疗冠心病的“基石”,在临床上广泛使用。然而,临床大数据结果发现,心血管药物的基石他汀容易造成副作用——糖耐量异常。但他汀类药物引起葡萄糖代谢紊乱的机理尚不明确。在袁祖贻教授指导下,课题组聚焦他汀同肠道菌群的交互作用开展了深入探索。通过测定人群队列的菌群变化,发现他汀类药物能够引起糖代谢紊乱、胰高血糖素样肽-1(GLP-1)异常降低和胰岛素抵抗,提示作用机制可能与GLP-1存在关联。研究团队基于宏基因组学和代谢组学联合分析的方法,探究肠道菌群及其代谢物与他汀导致糖稳态失调的相互作用,发现肠道菌群(梭状芽孢杆菌)通过降低鹅去氧胆酸(CDCA)向熊去氧胆酸(UDCA)转化从而抑制GLP-1水平。并通过多个动物疾病模型,验证了“他汀类药物通过降低肠道梭状芽孢杆菌来抑制UDCA水平加重胰岛素抵抗”这一分子机制(图1)。随后,对服用他汀类药物的患者进行熊去氧胆酸的临床干预治疗,发现联合治疗方案能够增加患者GLP-1水平,改善胰岛素抵抗。该研究揭示了他汀通过肠道菌群-胆汁酸稳态导致糖稳态失调的新机制,并通过临床试验显示了他汀联合熊去氧胆酸的潜在临床应用价值,为降脂治疗提供了新策略。该研究发表于《细胞•代谢》(Cell Metabolism)杂志。
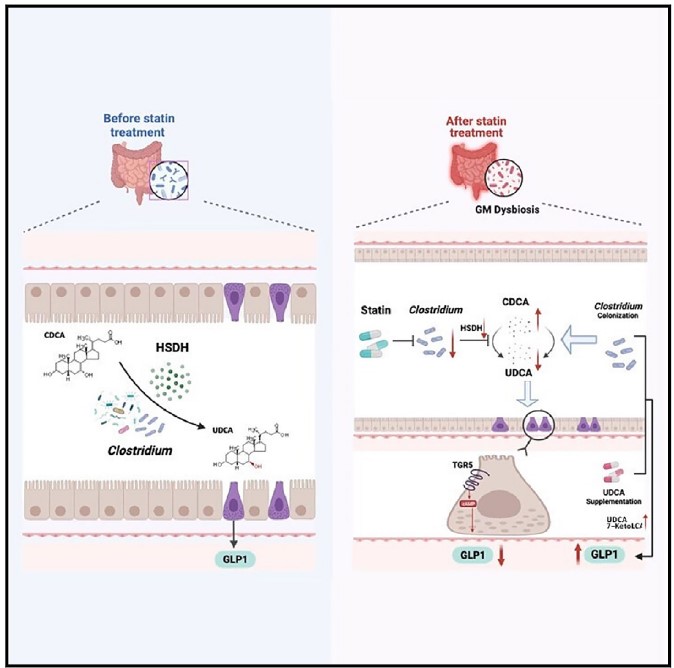
图1. 他汀通过肠道菌群造成糖耐量异常
阿司匹林亦心血管药物基石。然而,超过90%服用阿司匹林的患者会出现肠道副作用。传统观点认为阿司匹林造成的肠道环氧合酶活性抑制介导其损伤作用。但近期研究提示肠道菌及代谢也发挥作用,但具体机制不明。在袁祖贻教授指导下,课题组发现阿司匹林造成了肠道菌群失衡,减少了益生菌和一些胆汁酸的产生,从而抑制肠道干细胞的自我更新和肠道黏膜的修复功能(图2)。课题组建立阿司匹林干预的临床队列,深入探索肠道菌和代谢谱变化,发现我们发现一种益生菌——戈式副拟杆菌(P. goldsteinii)——生长受到口服阿司匹林的明显抑制。进一步的代谢组学分析显示,P.goldsteinii的胆汁酸代谢产物,包括熊去氧胆酸(UDCA)和7-酮石胆酸(7-keto-LCA),均具有保护肠道通透性、促进肠道黏膜损伤修复和保护肠道干细胞功能的重要作用。课题组发现发现7-酮石胆酸是一种未被报道过的胆汁酸受体抑制剂,能够激活肠道自我更新,抵抗阿司匹林造成的肠道损伤。补充戈式副拟杆菌或7-酮石胆酸,能够显著改善阿司匹林诱发的肠道副作用。该研究发表于《细胞•宿主和微生物》(Cell Host Microbe)杂志。
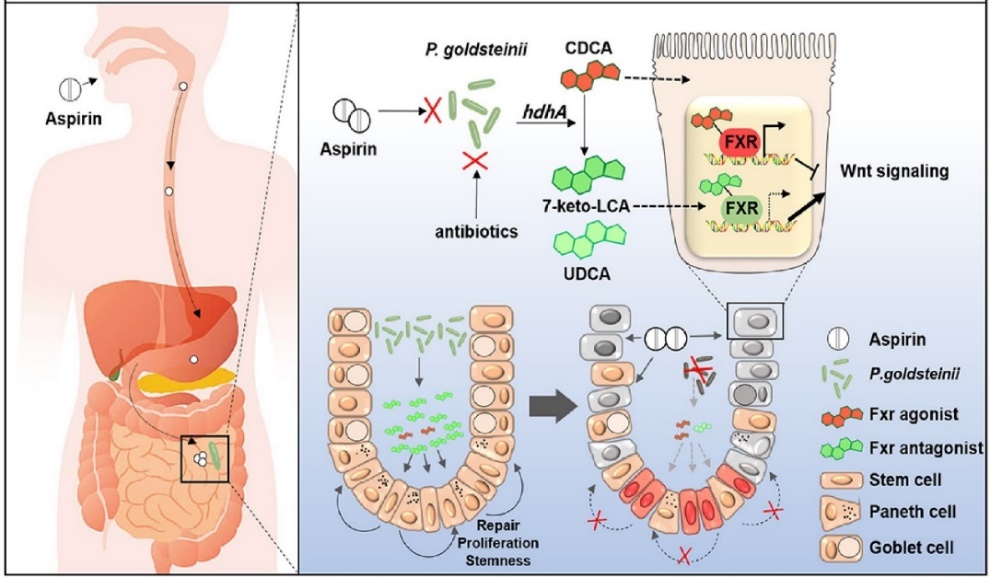
图2阿司匹林通过肠道菌群造成肠道微环境紊乱。Aspirin,阿司匹林;P.goldsteinii,戈氏副拟杆菌;hdhA,一种胆汁酸代谢酶;CDCA,鹅脱氧胆酸;UDCA,熊去氧胆酸;FXR,法尼醇受体X;Stem cell,干细胞;Paneth cell,潘氏细胞;Goblet Cell,杯状细胞。
袁祖贻教授,西安交大一附院心血管学科领军人,担任心血管病医院院长、心血管内科主任等职务,国家杰青获得者。长期致力于冠心病的临床及机制研究。在袁祖贻教授带领下,2023年专科在冠脉PCI手术方面例数逾8000例,是学科临床诊疗能力的有力证明,同时也展现了专科在区域内的影响力。团队在专科发展和胸痛中心建设方面发挥了关键作用,通过建立陕西省胸痛中心联盟,推动了地区胸痛急救网络的建设,提升了区域心血管急重症的救治水平,赢得了西北地区广大患者的认可。

吴岳教授长期致力于心血管代谢、肠道菌群等领域研究,主持国家重点研发计划等,主持开展多项创新性临床研究,创新性开展他汀类药物联合熊去氧胆酸的临床研究,有望解决他汀治疗过程中导致糖尿病的实际难题。此外,在罕见病治疗领域也是取得突破性进展。吴岳教授团队在全球首次利用腺相关病毒(AAV)治疗家族性高胆固醇血症HoFH。目前已有5例患者入组临床试验,低密度脂蛋白降幅显著,最新一例患者LDL胆固醇从12mmol/L降至1.9mmol/L,这一创新性治疗措施为该疾病提供了全新的治疗方向。
王胜鹏教授,国家优青,主持了国家自然科学基金面上项目、国际(地区)合作与交流项目,科技部战略发展项目等,致力于血管及代谢疾病的力学调控机制,在国际权威学术期刊发表研究论文32篇,14篇影响因子>10,累计影响因子265,以第一或共同通讯作者在Blood、JCI、Nat Commu (2篇)、Journal of Hepatology、Cir Res等杂志发表论文12篇,在机械力受体发现、高血压及肥胖的力学调控方面取得了一系列突破进展。
郭宁教授在复杂冠心病的诊治和研究领域具有良好的工作基础,目前主持的IVUS-CKD大型多中心随机对照研究,深入探讨IVUS指导在优化CKD患者PCI术中是否获益,研究结果将有望填补现有循证医学空白,为CKD患者冠心病诊疗提供决策支持,具有重要的临床意义。郭宁教授也主持了基于超高清双频IVUS成像系统的首例PCI患者入组,这项以我院心内科作为主研究单位的项目是全球首个基于超高清双频IVUS系统的临床研究,标志着超高频IVUS技术正式从科学研究走向临床应用新阶段,反应了专科在医疗技术创新领域的实力。
在心血管学科的探索之路上,西安交通大学第一附属医院心内科在袁祖贻教授的带领下,不仅致力于提升临床诊疗水准和增强专科的区域影响力,同时也深耕科研探索和临床成果的转化,结出累累硕果。展望未来,心内科团队将继续以患者为中心,推进科研创新,并将创新成果转化为提升临床服务的实策,确保患者真正受益,为守护心血管健康贡献力量。
原文链接:
Http://doi.org/10.1016/j.cmet.2023.12.027
Http://doi.org/10.1016/j.cmet.2023.12.027
